Cuando el joven doctor Louis Pasteur, a la sazón profesor del instituto de secundaria de Dijon, se enfrentó a su primer proyecto de investigación en solitario pensó que lo primero que necesitaba era una profunda preparación en cristalografía práctica. Decidió que lo mejor que podía hacer era estudiar sistemáticamente las formas cristalinas, repetir todas las mediciones y comparar sus resultados con los publicados. Uno de los estudios cristalográficos que decidió repetir fue el de 1841 de Frédéric Hervé de la Provostaye.
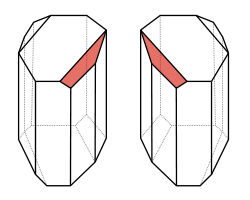
Pasteur fue muy meticuloso en la repetición de los experimentos. Esta meticulosidad tuvo su premio en el descubrimiento de algo que aparentemente había escapado tanto al ojo de Mitscherlich como al del propio de la Provostaye: aparecían caras hemiédricas en los cristales de tartrato de sodio y amonio. Sin embargo los cristales del racemato también tenían caras hemiédricas; la muestra bruta estaba formada en realidad por una mezcla de caras hemiédricas izquierdas y derechas.
Pasteur, en vez de anotar el dato y seguir con otra cosa, decidió investigar un poco. Con ayuda de una lupa y unas pinzas separó los cristales diestros y los zurdos, y preparó disoluciones con ellos. Para su sorpresa la disolución de zurdos era levorrotatoria y la de los diestros dextrorrotatoria. Si disolvía cantidades iguales de zurdos y diestros la disolución resultante era ¡ópticamente inactiva!
A continuación Pasteur decidió que tenía que comprobar la composición química de los cristales zurdos y diestros. Para ello obtuvo los ácidos libres a partir de las sales: el diestro era idéntico en todo al tartárico, el zurdo era en todo el tartárico pero con actividad óptica inversa.
Con todos estos datos el investigador de 25 años llegó a las siguientes conclusiones:
a) El ácido racémico no es un compuesto puro, sino una mezcla de iguales cantidades de ácido tartárico zurdo y diestro, que se diferencian tan sólo en su actividad óptica. La rotación óptica de los dos compuestos se cancela y, por lo tanto, la mezcla es inactiva.
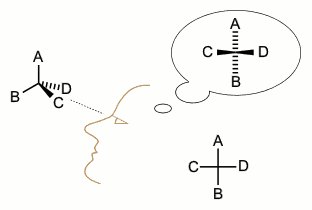
b) La actividad óptica de los compuestos orgánicos, sus disoluciones, y los líquidos es el resultado de la falta de simetría (Pasteur usaba la palabra disimetría) de las moléculas.
c) La actividad óptica de los cristales cuyas disoluciones (o fundidos) son ópticamente inactivos como, por ejemplo, el cuarzo o el clorato de sodio, se debe al empaquetamiento disimétrico de moléculas simétricas.
d) Al igual que sus cristales, las moléculas diestra y zurda del ácido tartárico eran imágenes especulares (enantiómeros).
Pasteur era muy consciente de la trascendencia de su descubrimiento y de su insignificancia dentro de la comunidad científica francesa. Por ello la forma en que decidiese comunicar sus resultados era de la mayor importancia. Así que, en vez de intentar publicar directamente, escribió a la única persona capaz de entender su trabajo y con influencia suficiente para conseguir una publicación con repercusión: Jean-Baptiste Biot, a la sazón con 74 años, a punto de dejar su cátedra en la Facultad de Ciencias de París y miembro de más de 20 academias científicas europeas y americanas.
Biot reconoció la importancia del descubrimiento inmediatamente y se mostró dispuesto a comunicarlo a la Academia de Ciencias de París a la primera oportunidad. Pero, y en esto Biot demostró ser un científico cabal, no antes de que se reprodujese el experimento en su laboratorio, ensayo al que invitó a asistir a Pasteur.
Biot proporcionó a Pasteur muestras de ácido racémico, preparada por él mismo y en la que había comprobado la inactividad óptica, hidróxido sódico y amoniaco y le pidió que preparase, a partir de ellas, en su presencia, la sal doble de sodio y amonio. Una vez preparada, Pasteur abandonó el edificio y la disolución se dejó evaporar en el laboratorio de Biot en el Collège de France. Cuando se habían separado algo más de 30 g de cristales, Biot convocó de nuevo a Pasteur para que separase los cristales en su presencia. Biot en persona preparó las disoluciones para comprobar la actividad óptica de los mismos. En cuanto colocó en el polarímetro la disolución que debía ser levógira y acercó su ojo al visor, Biot exclamó tomando la mano de Pasteur:
¡Mi querido hijo, he amado tanto durante toda mi vida esta ciencia que siento mi corazón latir de júbilo!
La comunicación a la Academia se produjo ese mismo año de 1848. En los años siguientes, ya profesor universitario en Estrasburgo, Pasteur continuó con sus estudios de la asimetría molecular y cristalina de muchos compuestos, incluyendo los aspartatos y malatos ópticamente activos y los inactivos que se comprobaba que eran “mezclas racémicas”.
En 1853, mismo año en el que se le haría caballero de la Orden Nacional de la Legión de Honor, Pasteur consiguió preparar el tercer isómero del ácido tartárico, ópticamente inactivo, hoy llamado meso-tartárico.
El descubrimiento de Pasteur de la quiralidad molecular (este nombre, ideado por Lord Kelvin en los años ochenta del XIX se acabaría imponiendo frente a las disimetrías de Pasteur) añadió la tercera dimensión a la química y fue el comienzo de la estereoquímica. En las décadas siguientes el concepto de molécula creció de una fórmula (1D), a un grafo (2D) y, finalmente, a finales del XIX, a un objeto 3D.
El modelo tetraédrico para los enlaces del carbono de van’t Hoff y le Bel (1874), el modelo octaédrico de coordinación de Werner (1893) y el trabajo monumental de Emil Fischer sobre la estereoquímica de los azúcares y las proyecciones moleculares (años noventa del XIX) toman como punto de partida el trabajo cristalográfico de Pasteur.
Este texto es la décimotercera parte de la serie Notas para una breve historia de la cristalografía.
Referencias generales de la serie:
[1] Wikipedia (enlazada en el texto)
[3] Molčanov K. & Stilinović V. (2013). Chemical Crystallography before X-ray Diffraction., Angewandte Chemie (International ed. in English), PMID: 24065378
[4] Lalena J.N. (2006). From quartz to quasicrystals: probing nature’s geometric patterns in crystalline substances, Crystallography Reviews, 12 (2) 125-180. DOI:10.1080/08893110600838528
[5] Kubbinga H. (2012). Crystallography from Haüy to Laue: controversies on the molecular and atomistic nature of solids, Zeitschrift für Kristallographie, 227 (1) 1-26. DOI: 10.1524/zkri.2012.1459
[6] Schwarzenbach D. (2012). The success story of crystallography, Zeitschrift für Kristallographie, 227 (1) 52-62. DOI: 10.1524/zkri.2012.1453
Esta entrada es una participación de Experientia docet en el III Festival de la Cristalografía que organiza ::ZTFNews y en la XXXII Edición del Carnaval de Química que acoge Dimetilsulfuro.




Magnífica entrada, precisa, resumida y rigurosa al tiempo. No conocía la anécdota de Biot y Pasteur. Me ha encantado.
Es interesante como este trabajo pionero abrió una de las cuestiones no resueltas mas recalcitrantes de la Ciencia actual: ¿por qué somos homoquirales?
Y como curiosidad, los cloratos (sodico y potasico) se han usado bastante como modelo de procesos de ruptura de simetría 🙂